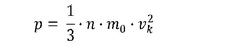Molekulaarfüüsika alused
Molekulaarfüüsika käsitleb soojusnähtusi arvestades aine siseehitust.
· Molekulaarfüüsikas nimetatakse molekuliks sellist aine osakest, mis osaleb molekulaarliikumises ehk soojusliikumises.
· Kõige lihtsama ehitusega aine on gaas.
· Gaaside molekulaarkineetilise teooria kolm põhieeldust:
1) Gaas koosneb molekulidest (osakestest)
2) Molekulid on pidevas kaootilises liikumises
3) Molekulide vahel on vastastikmõju
1 Mikrokäsitlus – eeldab aine koosnemist osakestest. Mikroparameetrid ei ole vahetult mõõdetavad vaid määratakse makroparameetrite kaudu.
Kasutatavad põhisuurused :
2 m – ainekoguse mass (näiteks gaas balloonis, õhupallis, autorehvis) ühik kg
m0 – aineosakese mass (sõltuvalt ainest kas aatomi või molekuli mass); kg
M – molaarmass, ehk ühe mooli mass ; kg/mol
N – aineosakeste (aatomite või molekulide) üldine arv aines, ühikuta
NA - Avogadro arv – aineosakeste arv iga aine ühes moolis, 1/mol
n – aineosakeste arv ruumalaühikus ehk kontsentratsioon 1/ m-3
ν – aine hulk ehk moolide arv ; mol
3 Ideaalne gaas :
1) molekulid on punktmassid
2) molekulide põrked anuma seintega on elastsed
3) molekulide vahel ei ole vastastikmõjusid, puuduvad tõmbe ja tõukejõud. Seega potentsiaalne energia puudub.
· Gaasi rõhk tekib molekulide põrgetest vastu anuma seina. Rõhk sõltub
- osakese massist
- osakeste kontsentratsioonist
- osakeste ruutkeskmisest kiirusest võrdeliselt.
Gaasi rõhku anuma seintele saab arvutada valemist, mida nimetatakse molekulaarfüüsika põhivõrrandiks.
Normaalrõhk: p=760 mmHg = 100 000 Pa
4. Temperatuur on suurus, mis iseloomustab keha või ainekoguse soojuslikku astet.
Temperatuur on molekulide keskmise kineetilise energia mõõt. Võime temperatuuri mõõta energia ühikutes.
Temperatuur on nii mikro – kui ka makroparameeter.
5. Temperatuuri mõõtmiseks kasutatakse erinevaid skaalasid. Igapäevases elus Celsiuse, teaduskeeles pigem Kelvini skaalat. Celsiuse järgi temperatuuri märkimisel kasutatakse tähist t, Kelvini järgi T. Seos kahe skaala vahel on järgmine:
T = t + 273
6. Absoluutne null, ehk madalaim võimalik temperatuur, on Kelvini skaala null, millele Celsiuse skaalal vastab -273,15 kraadi. See on temperatuur, mille korral seiskub igasugune aineosakeste liikumine. Kuna paigalseisust aeglasemalt liikuda pole võimalik, siis pole võimalik ka madalamate temperatuuride olemasolu. Tõenduseks see, et kuskil Universumis, milleni „ulatume“ tänapäevase teaduse abil pole madalamat temperatuuri mõõdetud.
Osakeste liikumise energia (keskmine kineetiline energia) sõltub temperatuurist järgmiselt:
K = 3/2 k T,
kus K on aineosakeste keskmine kineetiline energia, k on Boltzmanni konstant ja T temperatuur kelvini kraadides.
7. Seos rõhu ja temperatuuri vahel: p = nkT
Molekulaarfüüsika põhivõrrand:
| soojusõpetus.docx | |
| File Size: | 13 kb |
| File Type: | docx |
| mol.f._ülesanded.docx | |
| File Size: | 13 kb |
| File Type: | docx |
| gaas.jpg | |
| File Size: | 2297 kb |
| File Type: | jpg |
| tahke_keha.jpg | |
| File Size: | 2517 kb |
| File Type: | jpg |
| gaasi_rõhk.jpg | |
| File Size: | 2904 kb |
| File Type: | jpg |
Ülesanded
1. Leia järgmiste ühendite molaarmassid: NaCl, H2SO4, KMnO4.
2. Leia mitu mooli on 200g vett? Mitu vee molekuli on selles koguses?
3. Leia ühe vee molekuli mass.
4. Gaasi ruumala on 20 liitrit ja molekulide kontsentratsioon 1,6 x 1025 m-3 . Leia molekulide arv ja ainehulk moolides.
5. Leia keskmine kiirus ja ruutkeskmine kiirus molekulidele, mille kiirused on 200 m/s, 220 m/s, 260 m/s ja 400 m/s.
6. Leia vesiniku molekuli ruutkeskmine kiirus kui rõhk on 120 kPa ja kontsentratsioon 4 x 1024 m-3 .
7. Teisenda temperatuurid:
-200 C =………..K 277 K = …………….C
-13 C =…………..K 17 K = ………….C
8. Leia molekulide keskmine kineetiline energia temperatuuril 23 C.
9. Gaasi molekulide ruutkeskmine kiirus on temperatuuril 200 K 400 m/s. Leia ühe molekuli mass ja gaasi molaarmass.
10. Anumas on lämmastik temperatuuril 127 C. Leia molekulide keskmine kineetiline energia, ühe molekuli mass ja molekulide ruutkeskmine kiirus.
11. Balloonis on metaan ( CH4) rõhul 60 kPa. Arvuta molekulide kontsentratsioon, kui ruutkeskmine kiirus on 200 m/s.
12. Anumas ruumalaga 0,5 kuupmeetrit on 20 mooli veeauru rõhul 15 000 Pa. Arvuta 1) ühe molekuli mass 2) molekulide arv 3) gaasi mass 4) molekulide kontsentratsioon 5) molekulide ruutkeskmine kiirus 6) molekuli keskmine energia 7) gaasi temperatuur 8) rõhk
13. Balloonis ruumalaga 700 liitrit on 25 mooli lämmastikku rõhul 30 000 Pa . Vasta nende andmete põhjal eelmises ülesandes esitatud küsimustele.
2. Leia mitu mooli on 200g vett? Mitu vee molekuli on selles koguses?
3. Leia ühe vee molekuli mass.
4. Gaasi ruumala on 20 liitrit ja molekulide kontsentratsioon 1,6 x 1025 m-3 . Leia molekulide arv ja ainehulk moolides.
5. Leia keskmine kiirus ja ruutkeskmine kiirus molekulidele, mille kiirused on 200 m/s, 220 m/s, 260 m/s ja 400 m/s.
6. Leia vesiniku molekuli ruutkeskmine kiirus kui rõhk on 120 kPa ja kontsentratsioon 4 x 1024 m-3 .
7. Teisenda temperatuurid:
-200 C =………..K 277 K = …………….C
-13 C =…………..K 17 K = ………….C
8. Leia molekulide keskmine kineetiline energia temperatuuril 23 C.
9. Gaasi molekulide ruutkeskmine kiirus on temperatuuril 200 K 400 m/s. Leia ühe molekuli mass ja gaasi molaarmass.
10. Anumas on lämmastik temperatuuril 127 C. Leia molekulide keskmine kineetiline energia, ühe molekuli mass ja molekulide ruutkeskmine kiirus.
11. Balloonis on metaan ( CH4) rõhul 60 kPa. Arvuta molekulide kontsentratsioon, kui ruutkeskmine kiirus on 200 m/s.
12. Anumas ruumalaga 0,5 kuupmeetrit on 20 mooli veeauru rõhul 15 000 Pa. Arvuta 1) ühe molekuli mass 2) molekulide arv 3) gaasi mass 4) molekulide kontsentratsioon 5) molekulide ruutkeskmine kiirus 6) molekuli keskmine energia 7) gaasi temperatuur 8) rõhk
13. Balloonis ruumalaga 700 liitrit on 25 mooli lämmastikku rõhul 30 000 Pa . Vasta nende andmete põhjal eelmises ülesandes esitatud küsimustele.